Chemické reakcie sú všade okolo nás a prebiehajú neustále. Hoci si to často neuvedomujeme, sú základom mnohých procesov, ktoré nás obklopujú. Táto pomôcka sa zameriava na chemické zlučovanie, pričom objasňuje princípy a demonštruje ich na praktických príkladoch.

Čo sú Chemické Reakcie?
Chemické reakcie sú deje, pri ktorých reagujú jedna alebo viaceré látky (reaktanty, v novej terminológii edukty) a vzniká jeden alebo viac produktov. Látky, ktoré vstupujú do chemickej reakcie, nazývame reaktanty. V novej terminológii sa označujú aj ako edukty. Reaktanty môžu byť prvky alebo zlúčeniny. Najčastejšie sú aspoň dva, existujú však aj reakcie, v ktorých je iba jeden reaktant.
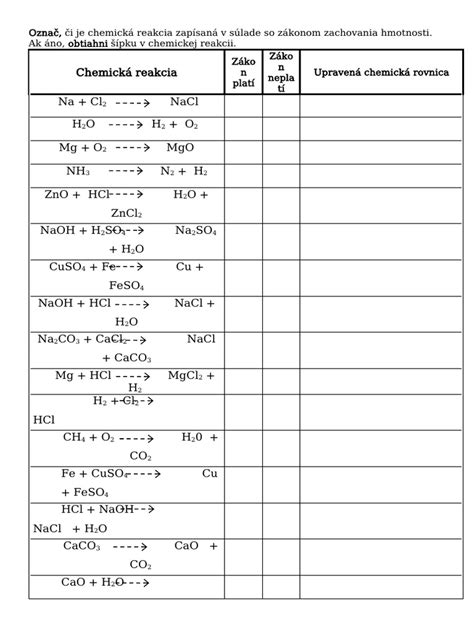
Dôležité je, že atómy pri chemickej reakcii nevznikajú ani nezanikajú; len sa preskupujú. Pri každej reakcii platí zákon zachovania hmotnosti. Ten hovorí, že počet a druh atómov reagujúcich látok sa pri reakcii nemení. Každý atóm, ktorý bol súčasťou reaktantov, je aj súčasťou produktov.
Vzorce reaktantov sa zapisujú na ľavú stranu rovnice, vzorce produktov na pravú stranu rovnice. Šípka ukazuje smer, ktorým chemická reakcia prebieha. Pri písaní chemických rovníc sa prvky zapisujú značkami a zlúčeniny vzorcami. Počet atómov každého druhu musí byť na oboch stranách rovnice zhodný. Šípka smeruje od reaktantov k produktom.
Delenie Chemických Reakcií
Chemické reakcie možno deliť podľa rôznych kritérií:
A. Podľa energetickej bilancie:
- Exotermické reakcie (exergonické): Tepelne neizolovaná sústava odovzdáva energiu svojmu okoliu tepelnou výmenou. Qm je záporná hodnota. Príklad: N2 + 3H2 → 2NH3 Qm = - 92,4 kJ.
- Endotermické reakcie (endergonické): Tepelne neizolovaná sústava spotrebúva energiu svojmu okoliu. Qm je kladná hodnota. Príklad: CaCO3 → CaO + CO2 Qm = + 178 kJ.
B. Podľa javového opisu anorganických látok:
- Skladné (syntetické): Reakcie, pri ktorých z niekoľkých reaktantov vzniká jeden produkt. Príklad: 2Na + Cl2 → 2NaCl.
- Rozkladné (analytické): Reakcie, pri ktorých z jedného reaktantu vzniká niekoľko produktov. Príklad: 2H2O → 2H2 + O2.
- Vytesňovacie (substitučné): Reakcie, pri ktorých jeden prvok v zlúčenine nahrádza iný.
- Podvojné zámeny (konverzie): Reakcie medzi roztokmi iónových zlúčenín, pri ktorých sa vymieňajú ióny a vzniká nerozpustná soľ. Príklad: AgNO3 + NaCl → AgCl + NaNO3.
C. Podľa javového opisu organických látok:
- Adičné: Zlučovanie 2 alebo viacerých častíc na jednu zložitejšiu, zánik násobnej väzby. Príklad: CH2=CH2 + Br2 → CH2Br-CH2Br.
- Eliminačné: Jedna častica sa štiepi na viac jednoduchších, vznik násobnej väzby. Príklad: CH3 - CH3 - H2 → CH2=CH2.
- Substitučné: Zánik jednej a vznik druhej väzby na tom istom atóme. Príklad: CH4 + Cl2 → CH3Cl + HCl.
- Prešmyky: Premiestnenie atómov, skupín alebo častí uhlíkového reťazca. Príklad: CH3 - CH2 - CH2 - CH3 → CH3 - CH - CH3 (izoizomér).
D. Podľa prebiehajúceho chemického deja:
- Oxidačno-redukčné (redoxné): Prenos elektrónov, ktorý sa prejaví zmenou oxidačného čísla niektorých prvkov. Pri oxidácii oxidačné číslo rastie, pri redukcii klesá. Príklad: Zn + CuSO4 → ZnSO4 + Cu.
- Acidobázické (protolytické, neutralizácia): Prenos protónov H+. Neutralizácia je reakcia kyseliny so zásadou, pričom vzniká soľ a voda. Pri neutralizácii reagujú oxóniové katióny s hydroxidovými aniónmi za vzniku molekúl vody. Príklad: HCl + NaOH → NaCl + H2O.
E. Podľa fázy v reakčnej sústave:
- Homogénne reakcie: Reaktanty aj produkty sú v rovnakej fáze, napr. látky v roztoku.
Chemické Zlučovanie a Redoxné Reakcie
Chemické zlučovanie je typ chemickej reakcie, pri ktorej sa dve alebo viac látok spája za vzniku jednej zložitejšej látky. Mnohé reakcie zlučovania sú zároveň redoxné reakcie, čo znamená, že pri nich dochádza k prenosu elektrónov medzi reaktantmi.
Ako vyvážiť redoxné reakcie - Prehľad praktického testu / skúšky zo všeobecnej chémie
1. Reakcia Horčíka s Oxidom Železistým
Táto reakcia demonštruje exotermickú reakciu zlučovania, ktorá produkuje teplo a svetlo.
Pomôcky:
- 1 g práškového manganistanu draselného KMnO4
- 3 g práškového oxidu železitého Fe2O3
- 2 g práškového horčíka
- Porcelánová miska, resp. miska s pieskom
- Kahan (plynový, resp. liehový)
- Glycerol
Postup:
- Zmiešajte práškový oxid železitý a horčík.
- Umiestnite zmes do väčšej misky s pieskom.
- Do stredu zmesi vytvorte jamku.
- Nakvapkajte 1 až 2 kvapky glycerolu do jamky.
- Zmes v miske zahrievajte plynovým kahanom asi 4 - 5 minúty.
Pozorovanie:
Reakcia sa iniciuje a prebieha exotermicky, pričom vzniká teplo a svetlo.
2. Horenie Horčíka
Horenie horčíka je klasický príklad chemickej reakcie zlučovania, pri ktorej sa horčík spája s kyslíkom zo vzduchu za vzniku oxidu horečnatého. Táto reakcia je sprevádzaná jasným svetlom a uvoľňovaním tepla.
Pomôcky:
- Kúsok horčíkovej pásky alebo práškový horčík
- Kahan (plynový, resp. liehový)
- Žiaruvzdorná podložka
Postup:
- Umiestnite horčíkovú pásku nad plameň kahana.
- Práškový horčík môžete nasypať do plameňa kahana.
Pozorovanie:
Horčík zhorí jasnožltým plameňom na biely oxid horečnatý.

3. Reakcia Zinku so Sírou
Táto reakcia demonštruje zlučovanie dvoch pevných látok za vzniku sulfidu zinočnatého.
Pomôcky:
- 8 g práškového zinku
- 4 g práškovej síry
- Porcelánová miska, resp. miska s pieskom
- Kahan (plynový, resp. liehový)
- Zápalná šnúra alebo klinec
Postup:
- Navážime práškový zinok a práškovú síru.
- Premiešame, aby sa farebne zjednotili.
- Zmes umiestnime do väčšej misky s pieskom.
- Iniciuje sa, napr. klincom.
Pozorovanie:
Vzniká pri nej plameň sýto žltého sfarbenia.
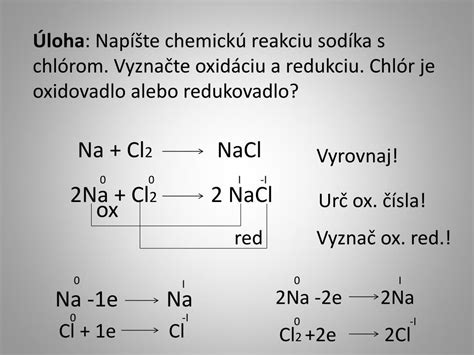
4. Reakcia Sodíka s Chlórom
Táto reakcia je prudká a demonštruje silnú afinitu medzi alkalickým kovom a halogénom.
Pomôcky:
- Kúsok sodíka (vo veľkosti hrášku)
- Plynový valec naplnený chlórom
- Lyžička na prenášanie sodíka
- Kahan (plynový, resp. liehový)
- Hodinové sklíčko
Postup:
- Osušíme kúsok sodíka vo veľkosti hrášku.
- Vložíme ho do plameňa kahana.
- Vložíme lyžičku so sodíkom do plynového valca s chlórom.
- Po chvíli valec uzavrieme hodinovým sklíčkom.
Pozorovanie:
Sodík reaguje s chlórom za vzniku bieleho chloridu sodného.
Faktory Ovplyvňujúce Priebeh Chemických Reakcií
Rýchlosť a priebeh chemických reakcií ovplyvňuje viacero faktorov:
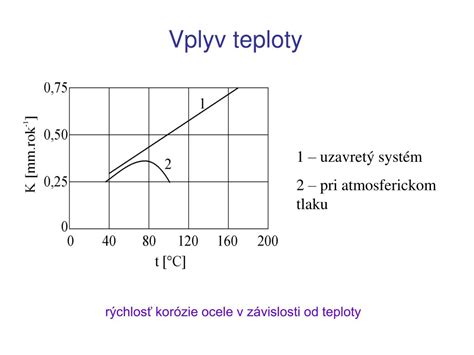
- Teplota: Vyššia teplota zvyčajne vedie k rýchlejšej reakcii, pretože častice majú viac energie na prekonanie aktivačnej energie.
- Koncentrácia reaktantov: Vyššia koncentrácia reaktantov zvyčajne vedie k rýchlejšej reakcii, pretože je viac častíc, ktoré sa môžu zraziť a zreagovať.
- Prítomnosť katalyzátora: Katalyzátor urýchľuje reakciu bez toho, aby sa spotreboval.
- Povrch reaktantov: Pri heterogénnych reakciách (reakcie medzi látkami v rôznych fázach) má väčší povrch reaktantov zvyčajne za následok rýchlejšiu reakciu.
- Miešanie: Miešanie zabezpečuje lepšie premiešanie reaktantov a odstraňuje lokálne koncentračné gradienty, čo môže urýchliť reakciu.
Dôležitosť Chemických Reakcií
Chemické reakcie sú nevyhnutné pre život a priemysel:
- Výroba energie: Spaľovanie palív, ako je drevo, uhlie a ropa, je chemická reakcia, ktorá uvoľňuje energiu.
- Výroba materiálov: Takmer všetky materiály, ktoré používame, sú výsledkom chemických reakcií.
- Trávenie potravy: Trávenie potravy je séria chemických reakcií, ktoré rozkladajú potravu na menšie molekuly, ktoré telo dokáže využiť.
- Dýchanie: Dýchanie je chemická reakcia, pri ktorej sa kyslík používa na oxidáciu glukózy za vzniku energie, vody a oxidu uhličitého.
- Fotosyntéza: Fotosyntéza je chemická reakcia, pri ktorej rastliny používajú slnečné svetlo na premenu oxidu uhličitého a vody na glukózu a kyslík.
Bezpečnosť pri Experimentoch
Pri vykonávaní chemických experimentov je dôležité dodržiavať bezpečnostné pokyny. Používajte ochranné okuliare, rukavice a pracujte v dobre vetranom priestore. Niektoré reakcie môžu byť nebezpečné a mali by sa vykonávať len pod dohľadom skúseného chemika. Je dôležité poznať vlastnosti a riziká chemikálií, s ktorými pracujete.
tags: #chemicke #zlucovanie #pomocka