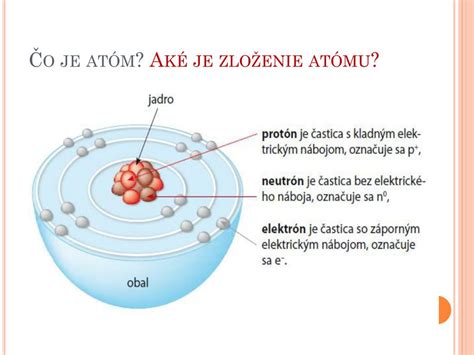
Atóm je základná stavebná častica chemických látok, chemicky najmenšia častica, ktorá môže vstupovať do chemickej reakcie. Skladá sa z dvoch častí: atómového jadra a elektrónového obalu.
Atómové jadro obsahuje protóny a neutróny, spoločne ich nazývame nukleóny. Protón je mikročastica, ktorá je nositeľom kladného elementárneho náboja. Neutrón je elektricky neutrálna mikročastica, veľkosťou a hmotnosťou sa rovná protónu.
Všetky atómy majú v jadre protóny a ich počet je charakteristický pre každý prvok. Počet protónov sa rovná počtu elektrónov a atóm je navonok elektricky neutrálny.
Elektrónový obal obsahuje elektróny. Elektróny sú mikročastice, ktoré sú nositeľom záporného elementárneho náboja.
Protónové, nukleónové a neutrónové číslo
Protónové (atómové) číslo Z udáva počet protónov v jadre atómu a počet elektrónov v elektrónovom obale (v elektricky neutrálnom atóme). Zhoduje sa s poradovým číslom prvku v Periodickej tabuľke prvkov (PSP).
Nukleónové (hmotnostné) číslo A udáva počet protónov a neutrónov (nukleónov) v jadre atómu. Zapisuje sa vľavo hore pri značke prvku.
Neutrónové číslo N udáva počet neutrónov v jadre. Platí vzťah A = Z + N.
Delenie prvkov na základe hodnôt Z a A:
- Nuklidy: súbor atómov, ktoré majú rovnaké protónové a nukleónové číslo.
- Izotopy: súbor atómov s rovnakým protónovým, ale rôznym nukleónovým číslom. Sú to atómy toho istého prvku, ktoré sa líšia počtom neutrónov v jadre atómu. Napríklad izotopy vodíka: 1H, 2H, 3H.
- Izobary: nuklidy rozličných prvkov, ktoré majú rovnaké nukleónové číslo a rozdielne protónové číslo.
Historický vývoj predstáv o zložení a štruktúre atómu
Vývoj predstáv o atóme prešiel dlhou cestou:
- V 5. storočí p.n.l. Demokritos a Leukipos prvýkrát použili pomenovanie atóm, z gr. atomos - nedeliteľný. Tvrdili, že každá látka je zložená z atómov, ktoré sú nezničiteľné, maličké, neviditeľné a nedeliteľné.
- V 18. storočí John Dalton vytvoril prvú ucelenú teóriu - Daltonovu atómovú teóriu. Jej nedostatkom bolo, že atóm považoval za nedeliteľný. Podľa Daltonovej teórie sú prvky zložené z malých, neviditeľných častíc - atómov. Atómy jedného prvku sú rovnaké, atómy rôznych prvkov sa líšia hmotnosťou a veľkosťou. Počas chemickej reakcie nastáva vzájomné spájanie, oddeľovanie a prestupovanie atómov. Spájaním atómov dvoch a viacerých prvkov vznikajú chemické zlúčeniny. Z tejto teórie priamo vyplýva zákon zachovania hmotnosti pri chemickej reakcii a zákon stálych hmotnostných pomerov.
- V 19. storočí vznikol Thomsonov model atómu. Thomson tvrdil, že atóm je guľa, v ktorej je kladný náboj vykompenzovaný záporným elektrickým nábojom. Vytvoril tak „model hrozienkového koláča“.
- Rutherfordov planetárny model - 1911. Rutherford bombardoval kovovú fóliu alfa časticami. Väčšina z nich kovovou fóliou prešla bez zmeny smeru a málo alfa častíc sa odrazilo späť. Z toho usúdil, že alfa častica musela naraziť na kladný elektrický náboj, ktorý zaberá veľmi malú časť atómu, ale v ktorom je sústredených až 99% hmotnosti atómu. Kladnú časť atómu nazval jadro. Dnes vieme, že priemer jadra atómu je 10 000 až 100 000-krát menší ako priemer celého atómu. Rutherford vytvoril planetárny model atómu, podľa ktorého okolo kladne nabitého jadra obiehajú záporne nabité elektróny ako planéty okolo Slnka.
- Bohrov model atómu - 1913. Podľa Rutherforda sa žiarenie, ktoré vychádzalo z atómu, vysvetľovalo tak, že elektrón vyžaruje sústavne svoju energiu pri pohybe okolo jadra. V dôsledku toho sa malo pozorovať spojité spektrum vysielaného žiarenia a elektrón by sa mal po špirálovitej dráhe zrútiť do jadra. Bohrov model tvrdil, že elektrón sa v atóme nachádza len v stavoch s určitou energiou. Chápeme to tak, že elektrón sa môže pohybovať okolo jadra len po takých kruhových dráhach, ktorých dĺžka sa rovná celistvému násobku vlnovej dĺžky elektrónu (2πr = n.λ). Atóm vyžaruje energiu, iba keď elektrón preskakuje z vyššej energetickej sféry na nižšiu. Rozdiel energií sa vyjadruje ΔE = E2 - E1, pričom E2 > E1.
- Kvantovo-mechanický model atómu (1924 - 27). Vytvorili ho štyria fyzici - zakladatelia kvantovej fyziky - Louis de Broglie, Ernest Schrodinger, Heisenberg a Max Born.
Kvantovo-mechanický model atómu a kvantové čísla
Kvantovo-mechanický model atómu hovorí, že pre elektrón nemôžeme v danom časovom okamihu určiť súčasne presnú polohu a hybnosť. Tento model umožňuje vypočítať pravdepodobnosť, s akou sa elektrón vyskytuje v určitej oblasti atómu. Výpočet tejto pravdepodobnosti výskytu elektrónu v okolí bodu daného súradnicami x,y,z v čase t nám umožňuje Schrodingerova rovnica pre vlnovú funkciu Ψ (psí).
Stav elektrónu v atóme opisujú štyri kvantové čísla, ktoré charakterizujú stav elektrónu v orbitale.
- Hlavné kvantové číslo - n: Vyjadruje energiu a veľkosť orbitalu, číslo sféry, na ktorej sa elektrón nachádza. Nadobúda celočíselné hodnoty 1, 2, ...7. Elektrónové vrstvy sa označujú aj veľkými písmenami K, L, M, N, O, P, Q.
- Vedľajšie kvantové číslo - l: Udáva tvar a energiu orbitalu. Nadobúda hodnoty od 0 do (n-1).
- Magnetické kvantové číslo - m (niekedy označované ml): Udáva smerovú orientáciu orbitalu v magnetickom poli. Jeho hodnota je daná číslom l. Pre dané l nadobúda magnetické kvantové číslo hodnoty m = -l,.., 0,...+l to jest (2l+1 hodnôt).
- Spinové číslo - s (niekedy označované ms): Určuje spin elektrónu, teda smer rotácie elektrónu okolo vlastnej osi. Má dve hodnoty s = ½ alebo s = -½. Ak elektrón rotuje v smere zľava doprava, s = ½, ak elektrón rotuje v smere sprava doľava, s = -½. Charakterizuje samotný elektrón, nie orbitál!
Typy orbitalov
Orbitál je priestor, v ktorom sa s určitou pravdepodobnosťou vyskytuje elektrón v atóme. Orbitály sú charakterizované troma kvantovými číslami.
Typy orbitalov podľa vedľajšieho kvantového čísla:
- s - orbital: je guľovo symetrický. Nachádza sa na každej sfére v počte 1 kus. Maximálne môže obsahovať 2 elektróny.
- p - orbital: začínajú od druhej sféry L, sú 3 a na každej sfére sú energeticky rovnocenné. Majú tvar priestorovej osmičky a sú na seba kolmé. V orbitále p sa môže vyskytovať najviac 6 elektrónov.
- d - orbital: začínajú od tretej sféry M a je ich 5. Na jednej sfére sú energeticky rovnocenné. Štyri majú tvar priestorového štvorlístka a jeden má tvar priestorovej osmičky s prstencom. Môže sa v ňom nachádzať až 10 elektrónov.
- f - orbital: začínajú od štvrtej sféry a na jednej sfére sú energeticky rovnocenné a je ich 7. Majú priestorovo zložitejšie tvary. Môže sa v ňom nachádzať až 14 elektrónov.
| Hlavné kvantové číslo (n) | Elektrónová vrstva | Vedľajšie kvantové číslo (l) | Typ orbitalu | Počet orbitalov | Maximálny počet elektrónov |
|---|---|---|---|---|---|
| 1 | K | 0 | s | 1 | 2 |
| 2 | L | 0 | s | 1 | 2 |
| 1 | p | 3 | 6 | ||
| 3 | M | 0 | s | 1 | 2 |
| 1 | p | 3 | 6 | ||
| 2 | d | 5 | 10 | ||
| 4 | N | 0 | s | 1 | 2 |
| 1 | p | 3 | 6 | ||
| 2 | d | 5 | 10 | ||
| 3 | f | 7 | 14 |
Elektrónová konfigurácia atómu a výstavbový princíp
Elektrónová konfigurácia atómu opisuje usporiadanie elektrónov daného atómu v jednotlivých orbitaloch. V atómovej fyzike a kvantovej chémii opisuje elektrónová konfigurácia rozmiestnenie elektrónov atómu, molekuly alebo inej fyzickej štruktúry v atómovom alebo molekulárnom orbitáli.
Výstavbový princíp (Aufbau princíp)
Orbitály s nižšou energiou sa zaplnia elektrónmi skôr ako orbitály s vyššou energiou. Energia orbitálu sa zvyšuje s rastúcou hodnotou súčtu hlavného (n) a vedľajšieho kvantového čísla (l). Ak majú dva rôzne orbitály rovnaký súčet n + l, potom je rozhodujúca hodnota hlavného kvantového čísla. Orbitál, ktorého hodnota n je menšia, má nižšiu energiu, a preto sa zaplní elektrónmi rýchlejšie.
Hundovo pravidlo
Hundovo pravidlo sa niekedy označuje i ako pravidlo maximálnej multiplicity. Pri zapĺňaní degenerovaných orbitalov (orbitaly s rovnakou energiou, napr. p-orbitaly) sa elektróny rozmiestňujú tak, aby čo najviac orbitalov obsahovalo jeden elektrón s paralelným spinom (predtým, ako sa začne s párovaním elektrónov v týchto orbitaloch).
Pauliho princíp
Pauliho princíp hovorí, že v atóme nemôžu existovať elektróny, ktoré majú zhodné všetky štyri kvantové čísla. Vždy sa musia odlišovať aspoň spinovým. Neexistujú 2 elektróny, ktoré by mali všetky kvantové čísla rovnaké. Na to, aby sme vedeli odlíšiť elektróny, ktoré sa nachádzajú v rovnakom orbitále aj jeho priestorovej orientácii, používame štvrté kvantové číslo, ktoré určuje smer rotácie elektrónu a má hodnoty +1/2, alebo -1/2.
Zápis elektrónovej konfigurácie
Na značenie elektrónovej konfigurácie používame niekoľko spôsobov. Môžeme si napísať hlavné kvantové číslo (1, 2, …) a za neho doplniť tvar orbitálu (s, p, d, f) podľa vedľajšieho čísla, pričom horný index udáva počet elektrónov v danom orbitale. Napríklad, elektrónová konfigurácia dusíka (N) so 7 elektrónmi je 1s2 2s2 2p3.
Ak chceme použiť grafické zobrazenie, môžeme si nakresliť štvorce, v ktorých každý elektrón znázorníme šípkou. V znázorňovaní orbitálov pomocou rámčekov sa všetky orbitály znázorňujú rovnako veľkými rámčekmi.
Tieto pravidlá platia, keď je atóm v základnom stave, teda má najnižšiu energiu. Keď mu energiu dodáme, dostane sa do excitovaného stavu.
Kvantové čísla, atómové orbitaly a elektrónové konfigurácie
Elektrónové vrstvy a Periodická tabuľka prvkov
Elektrónová vrstva (sféra) je tvorená orbitalmi, ktoré majú rovnakú hodnotu hlavného kvantového čísla a obsahujú elektróny.
Valenčná vrstva (sféra) je posledná vrstva v atóme, na ktorej ležia elektróny, je najvzdialenejšia od jadra. Valenčné elektróny sú elektróny, ktoré ležia na valenčnej vrstve. Plná valenčná vrstva znamená stabilitu prvku a jeho nereaktívnosť (vlastnosť vzácnych plynov).
Periodická tabuľka prvkov je rozdelená do vodorovných radov (periódy) a zvislých stĺpcov (skupiny). Periódy súvisia s polohou daného prvku v periodickej tabuľke a s jeho chemickými vlastnosťami.
- Prvá perióda (n = 1): označuje sa písmenom K. Nachádzajú sa tu dva prvky - vodík a hélium, pretože hlavnému kvantovému číslu n = 1 pripadá jediná hodnota vedľajšieho kvantového čísla l (l = 0). Z toho vyplýva, že prvá vrstva elektrónového obalu obsahuje iba jeden orbitál typu s. K jeho úplnému obsadeniu sú potrebné 2 elektróny.
- Druhá perióda (n = 2): označuje sa veľkým písmenom L. Táto perióda obsahuje celkovo osem prvkov. Tieto prvky majú úplne zaplnenú prvú vrstvu (2 elektróny v orbitály 1s). Zostávajúce elektróny a ich obaly sa nachádzajú v orbitáloch poslednej (v tomto prípade v druhej) vrstvy.
- Tretia perióda (n = 3): označuje sa veľkým písmenom M. Atómy prvkov tretej periódy majú svoje elektróny v orbitáloch 1s, 2s, 2p, 3s a 3p.
- Štvrtá perióda (n = 4): označuje sa veľkým písmenom N. V štvrtej perióde je situácia zložitejšia. Elektróny draslíku a vápniku zapĺňajú orbitál 4s, ktorý je súčasťou poslednej (štvrtej) vrstvy elektrónového obalu. Potom nasleduje desať prvkov (od skandia až po zinok), ktorého elektróny vstupujú do orbitálu 3d.
- V súčasnom stave má periodická tabuľka celkom 7 periód. Piata perióda sa označuje veľkým písmenom O, šiesta veľkým písmenom P a siedma veľkým písmenom Q.
tags: #vystavbovy #princip #pomocka