V chémii často používame pojmy ako „koncentrovaný roztok“, „zriedený roztok“ alebo „nasýtený roztok“, ktoré nám dávajú len základný prehľad o tom, či roztok obsahuje veľké alebo malé množstvo konkrétnej látky. Pojem „koncentrácia“ sa vzťahuje na mieru množstva danej látky obsiahnutej v konkrétnom roztoku.
Koncentrácia chemického roztoku vyjadruje množstvo rozpustenej látky prítomné v danom množstve rozpúšťadla alebo roztoku. Inými slovami, udáva, koľko látky (rozpustenej látky) je rozpustené v určitom objeme alebo hmotnosti roztoku. Výpočet a pochopenie koncentrácie sú nevyhnutné na predpovedanie výsledkov reakcií, vytváranie optimálnych podmienok pre chemické procesy a zabezpečenie presného vykonávania experimentov.
Jednotky vyjadrovania koncentrácie
V chémii existuje viacero spôsobov vyjadrenia koncentrácie, pričom výber vhodnej jednotky závisí od kontextu, povahy roztoku a jeho zložiek. Medzi najčastejšie používané jednotky patria:
- Molarita (M): Definovaná ako počet mólov rozpustenej látky na liter roztoku. Molarita je užitočná najmä pri reakciách zahŕňajúcich vodné roztoky a umožňuje jednoduché výpočty reakcií na základe objemov.
- Molalita (m): Definovaná ako počet mólov rozpustenej látky na kilogram rozpúšťadla.
- Normalita (N): Miera koncentrácie, ktorá sa často používa v acidobázickej chémii. Normalita meria gramový ekvivalent hmotnosti rozpustenej látky na liter roztoku.
- Hmotnostné percento (% w/w): Hmotnosť rozpustenej látky vydelená celkovou hmotnosťou roztoku a vynásobená 100 %.
- Objemové percento (% v/v): Objem rozpustenej látky vydelený celkovým objemom roztoku a vynásobený 100 %. Používa sa najmä pri roztokoch kvapalín v kvapalinách a v plynných zmesiach.
- Molový zlomok (x): Pomer počtu mólov zložky k celkovému počtu mólov všetkých zložiek v zmesi.
- Počet častíc na milión (PPM) a počet častíc na miliardu (PPB): Používajú sa pre veľmi zriedené roztoky a vyjadrujú počet jednotiek rozpustenej látky na milión, resp. miliardu jednotiek celkového roztoku.
- Formalita (F): Jednotka, ktorá vyjadruje hmotnosť rozpustenej látky v gramoch prítomnej v jednom litri roztoku. Formalita roztoku je počet vzorcových hmotností rozpustenej látky na liter roztoku.
Percentuálna koncentrácia
Percentuálna koncentrácia udáva, koľko hmotnostných dielov rozpustenej látky je zahrnutých v 100 hmotnostných dieloch roztoku. Inými slovami, je to počet gramov rozpustenej látky v 100 g roztoku.
Na odvodenie vzorca pre percentuálnu koncentráciu je potrebné pamätať na to, že hmotnosť roztoku (msol) obsahuje nielen hmotnosť rozpúšťadla (msolv), ale aj hmotnosť rozpustenej látky (ms):
msol = msolv + ms
Percentuálnu koncentráciu možno vypočítať podľa nasledujúceho vzorca:
Cp = (ms / msol) · 100 %
Ako vidíme zo vzorca, ak poznáme hmotnosť roztoku a hmotnosť látky, môžeme ľahko vypočítať percentuálnu koncentráciu. Každý vzorec, vrátane vzorca pre percentuálnu koncentráciu, je možné preusporiadať. Ak poznáme hmotnosť a percentuálnu koncentráciu roztoku, môžeme vypočítať hmotnosť rozpustenej látky. Podobne, ak poznáme percentuálnu koncentráciu a hmotnosť látky, môžeme vypočítať hmotnosť roztoku. Okrem preskupenia vzorca môžeme použiť aj vhodné proporcie.

Príklady výpočtu percentuálnej koncentrácie
Príklad 1: Koľko gramov cukru potrebujeme na prípravu 300 g 10 % roztoku?
Z návodu vieme, že hmotnosť roztoku je 300 g a jeho percentuálna koncentrácia je 10 %. Hmotnosť rozpustenej látky možno určiť dvoma spôsobmi.
Metóda 1. Preusporiadanie vzorca
ms = (Cp · msol) / 100 % = (10 % · 300 g) / 100 % = 30 g
Metóda 2. Použitím pomerov
100 g roztoku obsahuje 10 g cukru
300 g roztoku obsahuje x g cukru
x = (300 g · 10 g) / 100 g = 30 g
Obe metódy nás privedú k záveru, že na prípravu 300 g 10% roztoku bude potrebných 30 g cukru.
Príklad 2: V koľkých gramoch vody musíme rozpustiť 10 g látky, aby sme získali 50 % roztok?
Z návodu vieme, že hmotnosť látky je 10 g a percentuálna koncentrácia roztoku je 50 %. To znamená, že 100 g roztoku obsahuje 50 g látky. Hmotnosť roztoku možno určiť dvoma spôsobmi. Upozorňujeme, že hmotnosť roztoku sa nerovná hmotnosti rozpúšťadla. Na výpočet hmotnosti rozpúšťadla musíme od hmotnosti roztoku odpočítať hmotnosť látky.
Metóda 1. Preusporiadanie vzorca
msol = (ms · 100 %) / Cp = (10 g · 100 %) / 50 % = 20 g
msolv = msol - ms = 20 g - 10 g = 10 g
Metóda 2. Použitím pomerov
100 g roztoku obsahuje 50 g látky
x g roztoku obsahuje 10 g látky
x = (100 g · 10 g) / 50 g = 20 g
msolv = msol - ms = 20 g - 10 g = 10 g
Molarita (M)
Molarita (M) je jednotka koncentrácie definovaná ako počet mólov rozpustenej látky na liter roztoku. Pre výpočet molarity vydeľte počet mólov rozpustenej látky objemom roztoku v litroch:
M = (počet mólov rozpustenej látky) / (objem roztoku v litroch)

Molalita (m)
Molalita (m) je jednotka koncentrácie definovaná ako počet mólov rozpustenej látky na kilogram rozpúšťadla.
m = (počet mólov rozpustenej látky) / (hmotnosť rozpúšťadla v kilogramoch)

Normalita (N)
Normalita (N) je ďalšia jednotka koncentrácie, definovaná ako počet ekvivalentov na liter roztoku. Na výpočet normality vydeľte počet ekvivalentov rozpustenej látky objemom roztoku v litroch:
N = (počet ekvivalentov rozpustenej látky) / (objem roztoku v litroch)

Objemové percento
Objemové percento je jednotka koncentrácie definovaná ako objem rozpustenej látky na 100 jednotiek objemu roztoku. Objemový zlomok (φ) vyjadruje podiel objemu rozpustenej látky a celkového objemu roztoku. Používa sa najmä pri roztokoch kvapalín v kvapalinách a v plynných zmesiach.
Na výpočet objemového percenta, vydeľte objem rozpustenej látky objemom roztoku a vynásobte 100:
Objemové percento = (objem rozpustenej látky / objem roztoku) * 100 %
Objemový zlomok (φ) alebo (φ(B)) - objemový zlomok rozpustenej látky (B). Bezrozmerná veličina.
V(B) - objem rozpustenej látky (B) (v mililitroch alebo dm³).
V - celkový objem roztoku (v rovnakých jednotkách ako V(B)), pričom: V = V(B) + Vrozpúšťadla
Objemový zlomok možno vyjadriť aj v percentách. Vynásobením objemového zlomku (φ) číslom 100 získame objemové percento:
Φ(B) = φ(B) × 100 %
Objemové percento udáva, koľko objemových dielov rozpustenej látky pripadá na 100 dielov celkového objemu roztoku. Pri použití objemového zlomku je dôležité, aby boli všetky objemy merané pri rovnakej teplote, pretože objem látok závisí od teploty.

Mólový zlomok
Mólový zlomok je jednotka koncentrácie, ktorá predstavuje pomer počtu mólov zložky k celkovému počtu mólov všetkých zložiek v roztoku. Ak chcete vypočítať molový zlomok, vydeľte počet mólov zložky celkovým počtom mólov všetkých zložiek v roztoku:
Molový zlomok = (počet mólov zložky) / (celkový počet mólov všetkých zložiek)

Hustota roztokov a zmesí
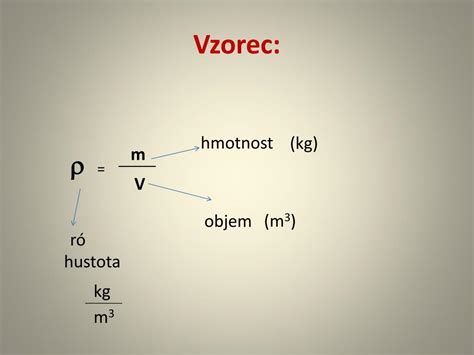
Hustota roztokov a zmesí (ρ) vyjadruje hmotnosť celého roztoku alebo zmesi vzťahovanú na jej objem. Na rozdiel od chemicky čistých látok, ktorých hustota je za daných podmienok konštantná, hustota roztoku závisí od jeho zloženia.
dsol = msol / vsol, kde msol je hmotnosť roztoku a Vsol je jeho hustota.
Ak poznáme objem a hustotu roztoku, vieme vypočítať jeho hmotnosť. Hustota roztoku je fyzikálna hodnota špecifická pre každú kvapalinu, ktorá definuje hmotnosť roztoku na jednotku objemu. Táto hodnota úzko súvisí s teplotou. Ak vieme, že hustota roztoku je 2,03 g/ml, tak vieme aj to, že 1 ml roztoku váži 2,03 g. Zvyčajne používame tieto jednotky hustoty: g/ml = g/cm³, g/l = g/dm³, ale existujú aj iné, napríklad kg/m³.
Premenné vo vzorci:
- ρ - hustota roztoku alebo zmesi (v jednotkách g/cm³ alebo g/dm³).
- m - celková hmotnosť roztoku alebo zmesi (v gramoch - g).
- V - objem roztoku alebo zmesi (v cm³ alebo dm³).
Hustota roztoku sa používa najmä pri výpočtoch koncentrácie, keď poznáme hmotnosť a potrebujeme určiť objem, alebo naopak. Zároveň umožňuje prechod medzi hmotnostnými a objemovými údajmi v roztokoch.
Medzi hustotou (ρ), hmotnostným zlomkom (w) a molárnou hmotnosťou (M) existuje priama súvislosť. Pre molárnu koncentráciu roztoku možno použiť nasledujúci vzťah:
c = (w · ρ) / M
Pomocou hustoty a hmotnostného zlomku teda môžeme vypočítať látkovú koncentráciu roztoku, ak poznáme molárnu hmotnosť látky. Hustota zmesi nie je aditívna - to znamená, že objem výsledného roztoku nemusí byť rovný súčtu objemov jednotlivých zložiek. Pri chemických výpočtoch sa preto vždy vychádza z meraného alebo zadaného objemu a hmotnosti konkrétneho roztoku.
Príklady výpočtu s hustotou
Príklad 3: Akú hmotnosť má 20 ml roztoku s hustotou 1,201 g/ml?
Metóda 1. Preusporiadanie vzorca
msol = dsol · Vsol = 1,201 g/ml · 20 ml = 24,02 g
Metóda 2. Použitím pomerov
1 ml roztoku má hmotnosť 1,201 g
20 ml roztoku má hmotnosť x g
x = (20 ml · 1,201 g) / 1 ml = 24,02 g
Obe metódy ukázali, že roztok s hustotou 1,201 g/ml a objemom 20 ml má hmotnosť 24,02 g.
Príklad 4: Koľko gramov soli obsahuje 10 ml 15 % roztoku, ak jeho hustota je 1,035 g/ml?
Metóda 1. Preusporiadanie vzorcov
msol = dsol · Vsol = 1,035 g/ml · 10 ml = 10,35 g
ms = (Cp · msol) / 100 % = (15 % · 10,35 g) / 100 % = 1,553 g
Metóda 2. Použitie proporcií
1 ml roztoku má hmotnosť 1,035 g
10 ml roztoku má hmotnosť x g
x = (10 ml · 1,035 g) / 1 ml = 10,35 g
100 g roztoku obsahuje 15 g soli
10,35 g roztoku obsahuje y g soli
y = (10,35 g · 15 g) / 100 g = 1,553 g
Obe metódy ukázali, že na prípravu 10 ml roztoku s Cp = 15 % a hustotou 1,035 g/ml musíme navážiť 1,553 g soli.
Ako pripraviť roztoky
Príklad 5: Aká je percentuálna koncentrácia roztoku, ktorý vznikne rozpustením 40 g látky v 200 ml etanolu s hustotou 0,78 g/ml?
Na výpočet môžeme použiť vzorec pre percentuálnu koncentráciu. Hmotnosť roztoku sa môže vypočítať sčítaním hmotností rozpustenej látky a rozpúšťadla. Hmotnosť rozpúšťadla nie je známa, ale poznáme jeho hustotu a objem, takže chýbajúce údaje možno vypočítať preskupením vzorca pre hustotu.
mrozpúšťadla = drozpúšťadla · Vrozpúšťadla = 0,78 g/ml · 200 ml = 156 g
msol = ms + mrozpúšťadla = 40 g + 156 g = 196 g
Cp = (ms / msol) · 100 % = (40 g / 196 g) · 100 % = 20,41 %
Zmiešavacia rovnica
Na výpočet koncentrácie alebo hmotnostného zlomku zložky roztoku vo výslednom roztoku, ktorý vznikol zmiešaním dvoch roztokov (zrieďovanie a zahusťovanie), sa používa zmiešavacia rovnica.
Tvary zmiešavacej rovnice:
- Pre výpočet s objemami, hustotami a hmotnostnými zlomkami: (V1 ρ1 w1 + V2 ρ2 w2 = V ρ w)
- Pre výpočet s objemami a koncentráciami látkového množstva: (c1 V1 + c2 V2 = c V)
Premenné vo vzorcoch:
- V1, V2, V - objemy roztokov.
- ρ1, ρ2, ρ - hustoty roztokov.
- w1, w2, w - hmotnostné zlomky roztokov.
- c1, c2, c - koncentrácie látkového množstva roztokov.
Výsledný objem roztoku nemusí byť vždy súčtom objemov zložiek.
Postup pri zrieďovaní roztoku:
- Používa sa rozpúšťadlo s (w = 0).
- Použije sa zmiešavacia rovnica na výpočet potrebných objemov alebo hmotností roztokov.
Postup pri zahusťovaní roztoku:
- Pridáva sa rozpustená látka, ktorá sa považuje za roztok s (w = 1).
- Použije sa zmiešavacia rovnica na výpočet potrebných hmotností alebo objemov roztokov.
Látkové množstvo a molárna hmotnosť
Pri chemických výpočtoch aj zápisoch chemických reakcií (chemických rovníc) niekedy potrebujeme vedieť, o aké množstvo látky ide. Dalo by sa to počítať na atómy alebo molekuly, ale to je veľmi nepraktické. V chémii máme tiež veličinu, ktorá vyjadruje počet atómov v látke. Táto veličina sa nazýva látkové množstvo. Značka látkového množstva je n a jeho jednotka je mól (značka tejto jednotky je mol). 1 mól obsahuje približne 6,022•1023 častíc. Toto číslo sa nazýva Avogadrova konštanta.
Rovnaké látkové množstvo rôznych látok má rôznu hmotnosť. Je to preto, lebo atómy, ktoré majú viac protónov, sú aj ťažšie. Na vyjadrenie konštantnej hmotnosti látky nám slúži veličina molárna hmotnosť (relatívna atómová hmotnosť). Jej značka je M a jej jednotka je gram na mól (g/mol).
Pre prvky je molárna hmotnosť uvedená v periodickej tabuľke. Pre zlúčeniny si ju vieme vypočítať.

Príklad výpočtu molárnej hmotnosti
Príklad: Vypočítajte molárnu hmotnosť kyseliny sírovej:
Vzorec kyseliny sírovej je H2SO4. Z neho vyplýva, že jedna molekula obsahuje dva atómy vodíka, jeden atóm síry a štyri atómy kyslíka.
Vyhľadajte si teda molárnu hmotnosť vodíka, síry a kyslíka:
- M(H) = 1,01 g/mol
- M(S) = 32,07 g/mol
- M(O) = 16 g/mol
Spočítajte všetky molárne hmotnosti. Prvky, ktoré sa v zlúčenine nachádzajú viackrát, započítajte viackrát.
M(H2SO4) = 2 · M(H) + M(S) + 4 · M(O) = 2 · 1,01 + 32,07 + 4 · 16 = 2,02 + 32,07 + 64 = 98,09 g/mol
Homogénne a heterogénne zmesi
Zmesi vznikajú zmiešaním dvoch alebo viacerých chemicky čistých látok (zložiek zmesi). Zloženie zmesí nie je možné vyjadriť pomocou chemického vzorca. Vlastnosti zmesí závisia od zloženia a pomeru jednotlivých zložiek. Na oddeľovanie zložiek zo zmesí sa využívajú rôzne metódy, ktoré využívajú rozdielne fyzikálne vlastnosti zložiek.
Rozlišovanie medzi homogénnymi a heterogénnymi sústavami závisí od veľkosti rozptýlených častíc.
Zmesi sa môžu deliť na:
- Rôznorodé zmesi (heterogénne): Zložky je možné rozlíšiť voľným okom alebo pod mikroskopom (napr. žula, piesok s vodou, olej s vodou, pena). Nemajú rovnaké zloženie v celom objeme zmesi.
- Rovnorodé zmesi (homogénne): Zložky nie je možné rozlíšiť voľným okom ani pod mikroskopom (napr. zliatiny kovov, sklo, minerálna voda, ocot, vzduch). Majú rovnaké zloženie a vlastnosti v celom objeme zmesi.
Roztoky sú homogénne disperzné sústavy, v ktorých je dispergovaná látka rozptýlená v dispergujúcej látke vo forme častíc s veľkosťou molekúl alebo iónov. Zmesi môžu existovať v rôznych skupenstvách: pevné, kvapalné, plynné. Špeciálnym prípadom sú koloidné zmesi, ktoré sa nachádzajú na pomedzí homogénnych a heterogénnych zmesí.
tags: #vypocet #koncentracie #roztoku #pomocka