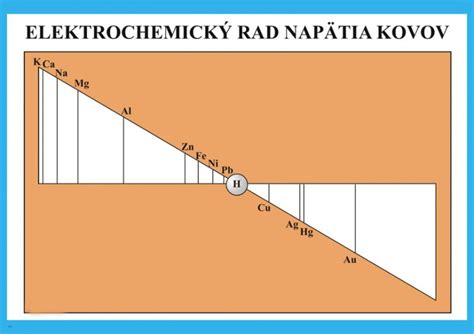
Elektrochemický rad napätia kovov, známy aj ako Beketovov rad (podľa Nikolaja Nikolajeviča Beketova) alebo rad reaktivity kovov, predstavuje systematické usporiadanie kovov. Tieto sú zoradené vzostupne podľa hodnôt ich štandardného elektródového potenciálu, ktorý sa vzťahuje na vodíkovú elektródu. Tento rad je kľúčový pre pochopenie oxidačno-redukčných vlastností daných kovov a predpovedanie priebehu chemických reakcií. Čím je kov viac vľavo v rade, tým lepšie odovzdáva elektróny (má redukčné vlastnosti). Naopak, prvky na pravej strane majú oxidačné vlastnosti a elektróny radi prijímajú.
Základy redoxných reakcií
Oxidačno-redukčné reakcie, skrátene aj redoxné reakcie, sú chemické reakcie, pri ktorých dochádza k zmene oxidačného čísla atómov alebo iónov.
- Oxidácia: Zväčšenie oxidačného čísla (strata elektrónov).
- Redukcia: Zníženie oxidačného čísla (príjem elektrónov).
Oxidácia a redukcia vždy prebiehajú súčasne ako neoddeliteľné deje. Ak sa jedna častica oxiduje (odovzdáva elektróny), musí byť prítomná iná častica, ktorá tieto elektróny prijme (redukuje sa).
Určovanie oxidačných čísiel
Na pochopenie redoxných reakcií je dôležité vedieť správne určovať oxidačné čísla prvkov. Oxidačné číslo je formálny náboj atómu prvku, ktorý by mal, ak by boli všetky väzby úplne iónové. Oxidačné číslo sa dá určiť aj pre prvky v kovalentných zlúčeninách, nielen v iónových. Hoci v skutočnosti pri kovalentných väzbách dochádza len k čiastočnému posunu elektrónov, oxidačné číslo sa určuje podľa rovnakých pravidiel.
Oxidačné číslo sa zapisuje dvoma hlavnými spôsobmi:
- Ako horný index pri symbole prvku v chemickom vzorci (napr. \( \text{Fe}_2^{III} \text{O}_3^{-II} \)). Tento zápis slúži na explicitné vyjadrenie formálneho náboja atómov a overenie celkovej neutrality zlúčeniny.
- Ako rímska číslica v zátvorke za názvom prvku v názvosloví zlúčeniny (napr. oxid železa(III)). Tento spôsob sa používa na jednoznačné určenie oxidačného čísla prvku, ktorý môže nadobúdať rôzne hodnoty.
V slovenskom názvosloví sa kladné oxidačné číslo kovu vyjadruje pomocou prípon (-ný, -natý, -itý, -ičitý atď.). Napríklad, prípona "-itý" v názve oxid železitý zodpovedá oxidačnému číslu \( +III \). Kladné oxidačné číslo sa v zátvorke nepíše so znamienkom \( + \).
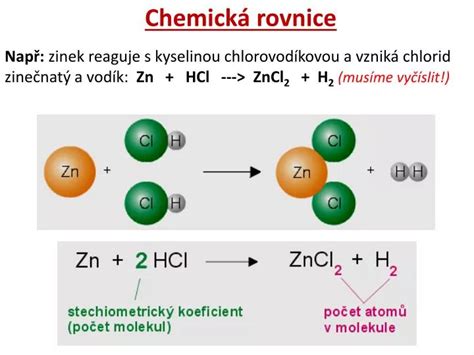
Príklad redoxnej reakcie:
\( \ce{Zn^0 + Cu^{2+} -> Zn^{2+} + Cu^0} \)
V tejto reakcii:
- Zinok (Zn) sa oxiduje, pretože odovzdáva dva elektróny; pôsobí ako redukovadlo.
- Ión meďnatý (Cu²⁺) sa redukuje, pretože prijíma dva elektróny; pôsobí ako oxidovadlo.
Na lepšie pochopenie prenosu elektrónov sa redoxná reakcia často rozpisuje na dve čiastkové reakcie:
\( \ce{Zn -> Zn^{2+} + 2e-} \)
\( \ce{Cu^{2+} + 2e- -> Cu} \)
Súčet týchto dvoch čiastkových reakcií dáva celkovú redoxnú reakciu:
\( \ce{Zn + Cu^{2+} -> Zn^{2+} + Cu} \)
Charakteristika kovov podľa radu napätia
Dôležitým referenčným bodom v elektrochemickom rade je vodík (\( E^\circ = 0{,}00 V \)). Podľa jeho postavenia môžeme kovy rozdeliť do dvoch kategórií:
- Neušľachtilé kovy: Nachádzajú sa pred vodíkom v rade. Majú tendenciu ľahko oxidovať, a preto môžu redukovať katióny vodíka z kyselín za vzniku plynného vodíka (H₂). Medzi tieto kovy patria napr. Li, Na, Mg, Al, Zn, Fe, Pb. Hoci niektoré z nich, napriek tomu, že stoja v Beketovom rade vľavo od vodíka, sa v roztokoch kyselín nerozpúšťajú. To je spôsobené inými faktormi - pasiváciou povrchu vrstvou kyselinám odolných oxidov, príp. iných zlúčenín daného kovu (napr. titán, ktorý je známy svojou mimoriadnou odolnosťou voči kyselinám, s výnimkou kyseliny fluorovodíkovej). V prírode sa vyskytujú len vo forme zlúčenín.
- Ušľachtilé kovy: Nachádzajú sa za vodíkom v rade. Majú nižšiu tendenciu oxidovať sa ako vodík, a preto nereagujú s neoxidujúcimi kyselinami za vzniku vodíka. Sú to napr. Cu, Ag, Au, Pt. Tieto kovy sa môžu vyskytovať aj v nezlúčenom stave.

Reakcie kovov s kyselinami
Neoxidujúce kyseliny
Kovy, ktoré sa v rade napätia nachádzajú pred vodíkom, majú väčšiu tendenciu oxidovať sa než vodík, a preto dokážu reagovať so zriedenými neoxidujúcimi kyselinami (napr. HCl, H₂SO₄). Neoxidujúce kyseliny uvoľňujú protóny (H⁺) pri reakciách, čo je ich charakteristická acidobázická vlastnosť. Ich anióny majú len veľmi malú alebo žiadnu tendenciu prijímať elektróny (redukovať sa), čiže sa nemenia.
Oxidujúce kyseliny
Oxidujúce kyseliny obsahujú anióny alebo centrálne atómy vo vysokých oxidačných stavoch, ktoré sa môžu ľahko redukovať (prijímať elektróny), čím sa menia a zároveň oxidujú daný kov v reakcii. Na rozdiel od neoxidujúcich kyselín, oxidujúce kyseliny môžu reagovať aj s ušľachtilými kovmi (teda kovmi, ktoré sú v elektrochemickom rade za vodíkom). Pri týchto reakciách nevzniká vodík, ale produkty oxidácie kyseliny, napríklad oxidy dusíka alebo síry.
Príkladmi silných oxidujúcich kyselín sú:
- Kyselina dusičná (HNO₃) - jedna z najsilnejších oxidujúcich kyselín, oxiduje aj ušľachtilé kovy.
- Koncentrovaná kyselina sírová (H₂SO₄) - v horúcom stave pôsobí ako silné oxidačné činidlo.
- Kyselina manganistá (HMnO₄) - extrémne silné oxidačné činidlo.
Príklad: Reakcia medi s koncentrovanou kyselinou dusičnou
Meď (Cu) sa nachádza v elektrochemickom rade kovov za vodíkom, a preto nereaguje s neoxidujúcimi kyselinami, ako je HCl. Avšak v reakcii s koncentrovanou kyselinou dusičnou (HNO₃) dochádza k oxidácii medi a vzniku dusičnanu meďnatého (Cu(NO₃)₂) a hnedého plynu oxidu dusičitého (NO₂).
\( \ce{Cu(s) + 4HNO3(aq) -> Cu(NO3)2(aq) + 2NO2(g) + 2H2O(l)} \)
Príklad: Reakcia zlata s lúčavkou kráľovskou
Zlato je extrémne ušľachtilý kov a nereaguje ani s kyselinou dusičnou, ani so sírovou. Rozpúšťa sa však v lúčavke kráľovskej, čo je zmes kyseliny dusičnej (HNO₃) a kyseliny chlorovodíkovej (HCl) v pomere 1:3.
Reakcia kyseliny a reaktívneho kovu (+ test na plynný vodík)
Vytláčanie prvkov z roztokov solí
Rad napätia kovov umožňuje predpovedať, či kov dokáže vytlačiť iný kov z roztoku jeho soli. Platí pravidlo, že kov dokáže vylúčiť ušľachtilejší kov z jeho roztoku. Spätná reakcia nie je možná. Čím väčší je rozdiel v postavení dvoch kovov v rade napätia, tým ochotnejšie a intenzívnejšie prebieha ich vzájomná redoxná reakcia.
Zovšeobecnením pravidla o vytláčaní/nevytláčaní vodíka je vytláčanie prvku, stojaceho v Beketovom rade vpravo, prvkom na ľavej strane.
Príklady reakcií na základe postavenia kovov v elektrochemickom rade napätia kovov:
| Reakcia | Priebeh |
|---|---|
| Mg + AgNO₃ → Ag + MgNO₃ | prebieha |
| Pb + Na₂SO₄ → | neprebieha |
| Cu + ZnSO₄ → | neprebieha |
| PbSO₄ + Na → Na₂SO₄ + Pb | prebieha |
| CuSO₄ + Zn → ZnSO₄ + Cu | prebieha |
| Ag + MgNO₃ → | neprebieha |
Experiment s meďou a železom
Špičku malej lyžičky síranu meďnatého v skúmavke rozpustite v objeme vody siahajúcom do výšky 2-3 cm. Klinec vložte do pripraveného roztoku. Ihneď sa pokryje tmavou, typicky červeno-hnedou vrstvou: meďou. Pomocou železného klinca sa podarí opätovne vyčarovať kovovú podobu medi len tak z ničoho nič, z vo vode rozpustných kryštálov síranu meďnatého. Tento proces nie je ojedinelým fenoménom, ale uplatňuje sa v ňom všeobecné pravidlo, ktoré hovorí: Kov dokáže vylúčiť ušľachtilejší kov z jeho roztoku. Spätná reakcia nie je možná. Takže, napríklad, nie je možné pomocou medeného drôtu z roztoku síranu železitého vytesniť železo.
V skúmavke do polovice naplnenej vodou rozpustite 1 lyžicu síranu meďnatého a do vzniknutého roztoku pridajte malé množstvo oceľovej vlny. Skúmavky uzavrite pomocou zátky a jej obsah poriadne pretrepte. Rovnako ako v prípade klinca sa na oceľovej vlne vytvorí červeno hnedý povlak. Skúmavku nechajte niekoľko minút odstáť. Roztok sa zmení farbu z modrej na matne zelenú. Roztok prefiltrujte do druhej skúmavky a pridajte doň 1 malú lyžičku uhličitanu sodného. Vznikne zelená usadenina. Do roztoku pridajte trochu peroxidu vodíka - farba roztoku sa zmení na hnedú - a spolu s varnou tyčinkou ho nad plameňom liehového horáka zohrievajte po dobu 1 - 2 minút. Do obsahu skúmavky pridajte lyžicu hydrogénsíranu sodného. Získate tak čisto žltý roztok. Zlúčenina FeSO₄, ktorú ste získali pozostáva z dvojnásobne kladne nabitého iónu železa (Fe²⁺) a dvojnásobne záporne nabitého síranového iónu (SO₄²⁻); v technickej terminológii sa nazýva síranom železnatým (odpovedá mu prípona II - natý). Reakciou s peroxidom vodíka vzniká zásaditý roztok síranu železitého (odpovedajúca prípona: III - itý), ktorý pozostáva z trojnásobne kladne nebitých iónov železa (Fe³⁺). Ióny Fe²⁺ zoxidovali na ióny Fe³⁺. Teraz už začínate tušiť, aký význam majú v chemickom názvosloví rímske číslice. Síran železnatý (II) obsahuje ióny Fe²⁺, zatiaľ čo síran železitý (III) obsahuje ióny Fe³⁺.
Redukčné činidlá v metalurgii
Uhlík je jedným z najčastejšie používaných redukčných činidiel v metalurgii. Jeho schopnosť redukovať oxidy kovov sa využíva predovšetkým v priemyselných procesoch, kde je potrebné získať čisté kovy z ich rúd. Táto metóda je ekonomicky výhodná, pretože uhlík je dostupný vo forme koksu alebo uhlia.
Príklad: Redukcia oxidu kremičitého uhlíkom
Elementárny kremík sa vyrába redukciou oxidu kremičitého uhlíkom pri vysokých teplotách:
\( \ce{SiO2 + 2C -> Si + 2CO} \)
Ak reakcia prebieha za prítomnosti železnej rudy, vzniká zliatina známa ako ferosilicium, ktorá sa používa pri výrobe ocele.
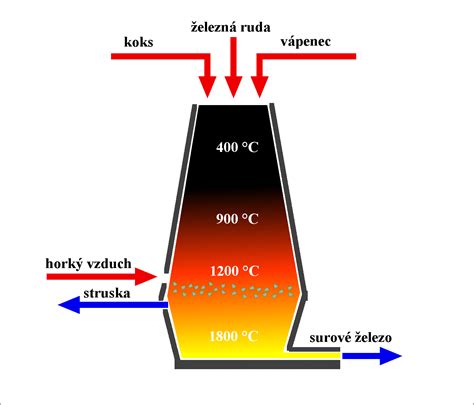
Príklad: Redukcia oxidov železa uhlíkom
Pri výrobe železa sa oxidy železa redukujú pomocou uhlíka alebo oxidu uhoľnatého v vysokých peciach. Metalotermická redukcia je proces, pri ktorom reaktívnejší kov (umiestnený vyššie v elektrochemickom rade kovov) pri vysokých teplotách redukuje kovovú zlúčeninu (napr. oxid) menej reaktívneho kovu. Menej reaktívne kovy sa často získavajú redukciou ich oxidov pomocou reaktívnejšieho kovu.
Aluminotermia
Hoci uhlík je efektívnym redukčným činidlom pre mnohé kovy, pri niektorých prvkoch nie je vhodný. Dôvodom je ich vysoká afinita ku kyslíku - tieto kovy by vytvorili stabilné karbidy alebo by sa uhlíkom nedali redukovať za bežných podmienok. Práve v takýchto prípadoch sa používa aluminotermia, kde hliník slúži ako silnejšie redukčné činidlo.
Aluminotermická reakcia je proces, pri ktorom sa hliník používa ako redukčné činidlo na získanie kovov z ich oxidov. Hliník má veľmi vysokú afinitu ku kyslíku, čo mu umožňuje odoberať kyslík menej reaktívnym kovom, čím sa tieto kovy uvoľňujú v elementárnej forme. Tento proces prebieha pri vysokých teplotách (až 3000 °C) a je silne exotermický, čo znamená, že počas neho vzniká veľké množstvo tepla. Výsledné produkty - redukovaný kov a oxid hlinitý - môžu byť v roztavenom stave v dôsledku extrémnej teploty reakcie.
Príklad: Redukcia oxidu železitého hliníkom (termitová reakcia)
Pri tejto reakcii sa oxid železitý (Fe₂O₃) redukuje pomocou práškového hliníka, pričom vzniká kovové železo a oxid hlinitý:
\( \ce{Fe2O3(s) + 2Al(s) -> Al2O3(s) + 2Fe(l)} \)
Reakcia prebieha veľmi rýchlo a je taká exotermická, že výsledné železo sa nachádza v roztavenom stave.
Elektrochemické články
Galvanické články a akumulátory
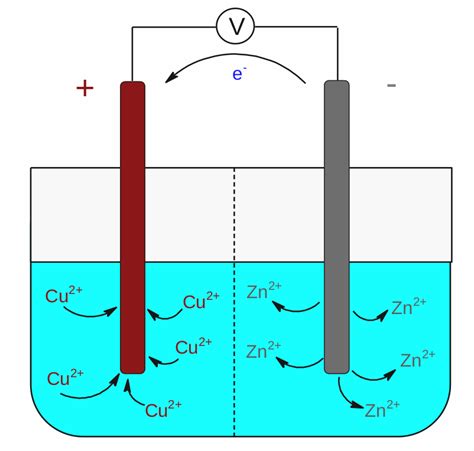
Princíp funkcie galvanických článkov je založený na spontánnych redoxných reakciách, pri ktorých sa chemická energia premieňa na elektrickú energiu. Na demonštráciu princípov fungovania galvanických článkov sa typicky používa tzv. Daniellov článok. Skladá sa zo zinkovej elektródy (anóda - záporná elektróda) ponorenej do roztoku zinočnatých katiónov (roztok ZnSO₄) a z medenej elektródy (katóda - kladná elektróda) ponorenej do roztoku meďnatých iónov (roztok CuSO₄). Chemická energia sa premieňa na elektrickú (na anóde sa rozpúšťa Zn, na katóde sa vylučuje meď).
- Anóda: Záporná elektróda, na ktorej prebieha oxidácia (uvoľňovanie elektrónov). Kov, ktorý má vyššiu tendenciu oxidovať sa (nachádza sa vyššie v rade napätia kovov), zvyčajne tvorí anódu. V Daniellovom článku: \( \ce{Zn(s) -> Zn^{2+}(aq) + 2e-} \)
- Katóda: Kladná elektróda, na ktorej prebieha redukcia (prijímanie elektrónov). Ióny kovu, ktorý má vyššiu tendenciu redukovať sa (nachádza sa nižšie v rade napätia kovov), zvyčajne prijímajú elektróny na katóde. V Daniellovom článku: \( \ce{Cu^{2+}(aq) + 2e- -> Cu(s)} \)
Elektróny uvoľnené na anóde prechádzajú vonkajším elektrickým obvodom ku katóde, čím vzniká jednosmerný elektrický prúd. Elektrolyt (roztok alebo tavenina obsahujúca ióny) umožňuje prechod iónov medzi elektródami, čím sa uzatvára elektrický obvod.
Akumulátory sú typom galvanických článkov, ktoré majú schopnosť byť po vybití opätovne nabité pripojením na externý zdroj jednosmerného napätia. Počas vybíjania fungujú ako bežné galvanické články, premieňajú chemickú energiu na elektrickú prostredníctvom spontánnych redoxných reakcií. Pri nabíjaní prebiehajú vynútené redoxné reakcie (elektrolýza), ktoré obnovujú pôvodné chemické látky v elektródach, čím sa akumulátor opäť nabije. Olovené akumulátory, bežne používané v automobiloch, pozostávajú z elektród z olova a oxidu olovičitého ponorených v roztoku kyseliny sírovej. Počas vybíjania olovo oxiduje na anóde a oxid olovičitý sa redukuje na katóde. Alkalické batérie sa používajú v prenosných elektronických zariadeniach.
Elektrolýza
Elektrolýza predstavuje redoxné reakcie, pri ktorých dochádza k rozkladu chemických látok prechodom jednosmerného elektrického prúdu roztokom alebo taveninou. Hoci elektrolýza je proces vynútený vonkajším zdrojom elektrickej energie, rad napätia kovov nám pomáha predpovedať, ktoré ióny budú preferenčne redukované na katóde a ktoré budú preferenčne oxidované na anóde.
- Na katóde (redukcia): Bude najľahšie redukovaný ten katión, ktorý sa nachádza nižšie v rade napätia kovov (má vyšší elektródový potenciál).
- Na anóde (oxidácia): Anióny s nižším štandardným oxidačným potenciálom (resp. vyšším štandardným redukčným potenciálom ich konjugovaných kyselín) budú oxidované ľahšie. Často však pri elektrolýze vodných roztokov dochádza k oxidácii vody na anóde za vzniku kyslíka.
Príklad: Elektrolýza vodného roztoku chloridu meďnatého (CuCl₂)
Vodný roztok chloridu meďnatého obsahuje katióny meďnaté (Cu²⁺) a anióny chloridové (Cl⁻). Voda v roztoku tiež disociuje na malé množstvo katiónov vodíka (H⁺ alebo presnejšie H₃O⁺) a aniónov hydroxidových (OH⁻).
- Katóda (redukcia): Na zápornú katódu sú priťahované kladné ióny (katióny) Cu²⁺ a H⁺. Podľa radu napätia kovov je redukcia iónov medi \( \ce{Cu^{2+} + 2e- -> Cu} \) ľahšia ako redukcia iónov vodíka \( \ce{2H^{+} + 2e- -> H2} \). Preto na katóde dochádza k vylučovaniu elementárnej medi: \( \ce{Cu^{2+}(aq) + 2e- -> Cu(s)} \)
- Anóda (oxidácia): Na kladnú anódu sú priťahované záporné ióny (anióny) Cl⁻ a OH⁻. Pri vyššej koncentrácii chloridových iónov sa prednostne oxidujú chloridové ióny za vzniku plynného chlóru: \( \ce{2Cl-(aq) -> Cl2(g) + 2e-} \)
Celková reakcia: \( \ce{CuCl2(aq) -> Cu(s) + Cl2(g)} \)
Elektrolýza soľanky je priemyselná výroba NaOH (mydlá a saponáty, papierenský priemysel, výroba hliníka, vlákna), H₂ (zváranie, stužovanie rastlinných olejov, raketové palivo, výroba amoniaku, hnojív), Cl₂ (kyselina chlorovodíková, dezinfekčné prostriedky, farbivá, úprava vody) v elektrolyzéri. Elektrolýza Al₂O₃ prebieha v železných komorách pokrytých grafitom (katóda), v tavenine ponorené uhlíkové anódy.
Reakcia kyseliny a reaktívneho kovu (+ test na plynný vodík)
Korózia
Korózia je fyzikálno-chemická reakcia medzi kovom a prostredím. Reakcie prebiehajúce pri styku železa s ušľachtilejším kovom vo vlhkom prostredí spôsobujú korodovanie železných predmetov. Vlhý vzduch a voda obsahujúca oxid uhličitý majú oxidačné účinky - železo ich vplyvom hrdzavie. Kombináciou železa s niekoľkými ďalšími kovmi do zliatiny získate nehrdzavejúcu oceľ užitočnú na výrobu, okrem iného, kuchynského náradia či laboratórnych pomôcok.